

Déplacement d'équilibre réactionnel. Un article de Wikipédia, l'encyclopédie libre.
Dans de nombreuses synthèses chimiques, l'un des principaux buts est d'améliorer le rendement. Lorsque ces synthèses sont des équilibres, comme dans le cadre de l'estérification, on cherche à déplacer ces équilibres de manière à augmenter le rendement. Ici sont réunies les principales lois qui régissent ces déplacements d'équilibres. Définitions[modifier | modifier le code] Soit un système physico-chimique dans un état d'équilibre. Loi de la tonométrie. Théorie des collisions. Un article de Wikipédia, l'encyclopédie libre.
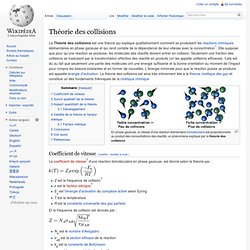
La Théorie des collisions est une théorie qui explique qualitativement comment se produisent les réactions chimiques élémentaires en phase gazeuse et qui rend compte de la dépendance de leur vitesse avec la concentration[1]. Elle suppose que pour qu'une réaction se produise, les molécules des réactifs doivent entrer en collision. Seulement une fraction des collisions se traduisent par la transformation effective des réactifs en produits (on les appelle collisions efficaces). Cela est dû au fait que seulement une partie des molécules ont une énergie suffisante et la bonne orientation au moment de l'impact pour rompre les liaisons existantes et en former de nouvelles. Loi de Raoult. Principe HSAB. Un article de Wikipédia, l'encyclopédie libre.
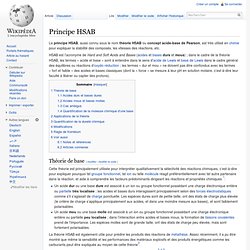
Le principe HSAB, aussi connu sous le nom théorie HSAB ou concept acide-base de Pearson, est très utilisé en chimie pour expliquer la stabilité des composés, les vitesses des réactions, etc. Théorie de base[modifier | modifier le code] Cette théorie est principalement utilisée pour interpréter qualitativement la sélectivité des réactions chimiques, c’est-à-dire pour expliquer pourquoi tel groupe fonctionnel, tel ion ou telle molécule réagit préférentiellement avec tel autre partenaire dans la réaction, et aide à comprendre les facteurs prédominants dirigeant les réactions et propriétés chimiques [1]: Un acide dur ou une base dure est associé à un ion ou groupe fonctionnel possédant une charge électronique entière ou partielle très localisée ; les acides et bases durs interagissent principalement selon des forces électrostatiques comme s'il s'agissait de charge ponctuelle.
Acides durs et bases dures[modifier | modifier le code] Loi de dilution d'Ostwald. Un article de Wikipédia, l'encyclopédie libre.
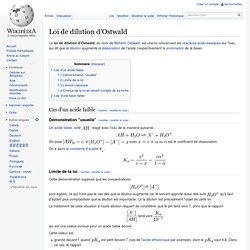
La loi de dilution d'Ostwald, du nom de Wilhelm Ostwald, est une loi concernant les réactions acido-basiques sur l'eau, qui dit que la dilution augmente la dissociation de l'acide (respectivement la protonation de la base). Cas d'un acide faible[modifier | modifier le code] Démonstration "usuelle"[modifier | modifier le code] Un acide faible, noté.
Règle de Markovnikov. Un article de Wikipédia, l'encyclopédie libre.
La règle de Markovnikov est une loi utilisée en chimie organique basée sur la règle de Zaïtsev. Elle a été formulée par le chimiste russe Vladimir Markovnikov en 1869[réf. nécessaire]. Loi des proportions multiples. Un article de Wikipédia, l'encyclopédie libre.
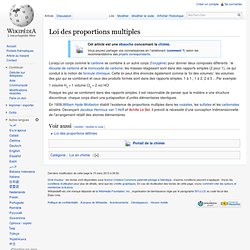
Lorsqu'un corps comme le carbone se combine à un autre corps (l'oxygène) pour donner deux composés différents : le dioxyde de carbone et le monoxyde de carbone, les masses réagissant sont dans des rapports simples (2 pour 1), ce qui conduit à la notion de formule chimique. Cette loi peut être énoncée également comme la ‘loi des volumes’: les volumes des gaz qui se combinent et ceux des produits formés sont dans des rapports simples: 1 à 1., 1 à 2, 2 à 3 …Par exemple: 1 volume H2 + 1 volume Cl2 = 2 vol HCl Puisque les gaz se combinent dans des rapports simples, il est raisonnable de penser que la matière a une structure discontinue, chaque corps étant une juxtaposition d’unités élémentaires identiques. En 1808,William Hyde Wollaston établit l’existence de proportions multiples dans les oxalates, les sulfates et les carbonates alcalins.
Loi des proportions définies. Un article de Wikipédia, l'encyclopédie libre.
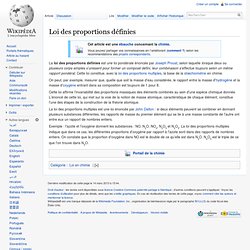
La loi des proportions définies est une loi pondérale énoncée par Joseph Proust, selon laquelle lorsque deux ou plusieurs corps simples s'unissent pour former un composé défini, leur combinaison s'effectue toujours selon un même rapport pondéral. Cette loi constitue, avec la loi des proportions multiples, la base de la stœchiométrie en chimie. On peut, par exemple, mesurer que, quelle que soit la masse d'eau considérée, le rapport entre la masse d'hydrogène et la masse d'oxygène entrant dans sa composition est toujours de 1 pour 8. Cette loi affirme l'invariabilité des proportions massiques des éléments combinés au sein d'une espèce chimique donnée.
Loi de Charles. Un article de Wikipédia, l'encyclopédie libre.
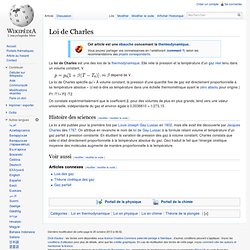
La loi de Charles est une des lois de la thermodynamique. Elle relie la pression et la température d'un gaz réel tenu dans un volume constant, V. , où dépend de V. La loi de Charles spécifie qu'« À volume constant, la pression d'une quantité fixe de gaz est directement proportionnelle à sa température absolue » (c'est-à-dire sa température dans une échelle thermométrique ayant le zéro absolu pour origine.) On constate expérimentalement que le coefficient β, pour des volumes de plus en plus grands, tend vers une valeur universelle, indépendante du gaz et environ égale à 0,0036610 = 1/273,15.
Histoire des sciences[modifier | modifier le code] La loi a été publiée pour la première fois par Louis Joseph Gay-Lussac en 1802, mais elle avait été découverte par Jacques Charles dès 1787. Voir aussi[modifier | modifier le code] Articles connexes[modifier | modifier le code] Loi d'homogénéisation isotopique. Un article de Wikipédia, l'encyclopédie libre.
La loi d'homogénéisation isotopique est un postulat, basé sur l'expérience, qui exprime le fait que dans le Système solaire, la répartition des isotopes d'un élément est constante en tout point géographique. Cette loi découle du brassage des éléments constitutifs de la matière au moment de la formation du Système solaire (« homogénéisation initiale »). Parmi les isotopes d'un élément, les plus abondants sont normalement les plus stables et souvent les plus légers. Toutefois, la répartition normale connaît quelques variations, selon les conditions locales. Ainsi, certains taux isotopiques seront plus ou moins élevés selon les conditions climatiques.
Déplacement d'équilibre réactionnel. Un article de Wikipédia, l'encyclopédie libre.
Dans de nombreuses synthèses chimiques, l'un des principaux buts est d'améliorer le rendement. Lorsque ces synthèses sont des équilibres, comme dans le cadre de l'estérification, on cherche à déplacer ces équilibres de manière à augmenter le rendement. Ici sont réunies les principales lois qui régissent ces déplacements d'équilibres. Règle de Hückel. Un article de Wikipédia, l'encyclopédie libre. Pour les articles homonymes, voir Hückel. En chimie, la règle de Hückel s'exprime ainsi : Loi de Hess. Un article de Wikipédia, l'encyclopédie libre. La loi de Hess est une loi de la thermochimie, élaborée par le chimiste suisse Germain Henri Hess.
Loi de Henry. Un article de Wikipédia, l'encyclopédie libre. À température constante et à saturation, la quantité de gaz dissous dans un liquide est proportionnelle à la pression partielle qu'exerce ce gaz sur le liquide. La concentration maximale d'un gaz en solution, en équilibre avec une atmosphère contenant ce gaz, est proportionnelle à la pression partielle de ce gaz en ce point. C’est-à-dire que si l'on est par exemple en un point où la pression est le double de la pression atmosphérique (c'est le cas dans l'eau à 10 m de profondeur), chaque gaz de l'air pourra se dissoudre 2 fois mieux qu'en surface.
Ceci explique le problème des plongeurs : en profondeur, l'azote de l'air (que le plongeur stocke puisque les cellules ne consomment que l'oxygène) a tendance à se dissoudre dans l'organisme du plongeur (entre autres le sang). Loi de Kohlrausch. Diffusion de la matière. Loi de l'ébulliométrie. Loi de la cryométrie. Théorie de Brønsted-Lowry. Gaz parfait. Un article de Wikipédia, l'encyclopédie libre. Cycles de Carnot pour un gaz parfait de Laplace monoatomique dans des diagrammes Volume-Pression (V,P) et Entropie-Température (S,T). Parce que les lignes isothermes et adiabatiques sont équidistantes au sens de la température absolue et de l'entropie, tous les losanges curvilignes élémentaires ont même aire. Loi d'Avogadro. Loi d'Arrhenius. Loi d'action de masse.