

Skyview Los Alamos, Los Alamos – Tarifs 2018. Les états de la matière et les changements d'état. On peut se représenter une substance pure, telle que l'eau, comme un ensemble de particules élémentaires trop petites pour être visibles à l'œil nu ou même avec les microscopes optiques les plus puissants.
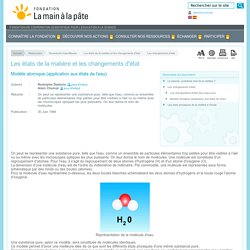
On leur donne le nom de molécules. Une molécule est constituée d'un regroupement d'atomes. Pour l'eau, il s'agit du regroupement de deux atomes d'hydrogène (H) et d'un atome d'oxygène (O). Les états de la matière et les changements d'état. Les corps purs peuvent exister sous différents états (solide, liquide et gazeux) selon les conditions de température et de pression.
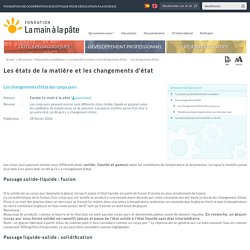
Lorsque la matière passe d’un état à un autre état, on dit qu’il y a changement d’état. Passage solide-liquide : fusion Si le solide est un corps pur (exemple la glace), lorsqu’il passe à l’état liquide, on parle de fusion franche ou plus simplement de fusion. La caractéristique de la fusion d’un corps pur est qu’elle se produit à une température donnée qui reste constante durant toute la durée du changement d’état. Ainsi si on met des glaçons dans un verre qui se trouve lui-même dans une pièce à température ambiante, on constate que le glaçon fond et que la température du verre contenant le glaçon et l’eau reste autour de 0° tant qu’il existe un petit bout de glaçon. Passage liquide-solide : solidification C’est ce qui se passe lorsque l’on met de l’eau dans le freezer du réfrigérateur ou dans un congélateur.
Passage liquide-gaz : vaporisation. Les états de la matière et les changements d'état. Une substance peut passer de l'état gazeux à l' état liquide ou solide, de l' état liquide à l'état gazeux ou solide, de l'état solide à l'état gazeux ou liquide ; c'est un changement d'état.
Cela signifie que, suivant les circonstances, un même corps peut se présenter sous forme solide, liquide ou gazeuse. Par exemple, l'eau peut exister sous ces différentes formes qui correspondent à des organisations moléculaires différentes (modèle de la matière). Les états de la matière et les changements d'état. Essayons de nommer tout ce qui se trouve dans le monde.
La liste s'allonge très vite. Tant de choses nous entourent ! On peut imaginer de les classer de bien des façons : d'après leur forme, leur couleur, leur odeur, leur taille, leur usage, etc. On distingue habituellement trois classes de corps : les solides, les liquides, les gaz. Les solides sont les plus faciles à reconnaître. On ne peut pas saisir un peu d'eau du bout des doigts.
Les liquides coulent. On peut saisir entre ses doigts un grain de sable. L'air, l'oxygène, le gaz de ville, le gaz carbonique, l'azote, le krypton.... sont des gaz. Densité et masse volumique. Une 1re façon de faire : Comparer les masses d'un même volume de substances différentes.
On essaye de trouver des objets solides de formes diverses qui ont le même volume (par exemple 75 cm3). La matière à différentes échelles. Dans le jardin à l’abandon de la rue Plumet où Marius et Cosette se donnent rendez-vous, tout un ensemble de structures naturelles grandes et petites coexistent, enchevêtrées et solidaires.
Cette solidarité est décrite avec emphase par Victor Hugo dans les Misérables, et pourrait servir d’introduction à notre excursion dans les échelles de la matière : Rien n’est petit en effet… L‘irradiation de l’astre profite à la rose… Qui donc peut calculer le trajet d’une molécule ? Que savons-nous si les créations de mondes ne sont point déterminées par des chutes de grains de sable ?
Qui connaît les flux et les reflux réciproques de l’infiniment petit et de l’infiniment grand ? Un ciron importe ; le petit est grand, le grand est petit ; tout est en équilibre dans la nécessité. Pascal avait déjà utilisé cette référence au ciron, un acarien parasite du fromage à peine visible à l’œil nu, pour illustrer l’infiniment petit(1).
Nous serons plus modestes ici. A propos de matières et matériaux : de la science à la technologie. On ne montrera jamais assez aux collégiens combien les progrès de la connaissance sur la matière doivent aux talents du scientifique, du « savant ».

La maîtrise de l’exercice de ces talents est multiple, notamment à travers l’observation, l’expérimentation, la modélisation ou encore les approches multidisciplinaires et multi-échelles. L’histoire des sciences racontée aux collégiens peut souvent se révéler le meilleur « outil » pour leur faire découvrir que les plus éminents de nos grands savants sont, le plus souvent, ceux qui ont su associer plusieurs de ces talents. Ainsi, intégrée dans un projet porté par toute une équipe pédagogique (professeurs de science et technologie, d’histoire, de français, etc.), l’histoire des sciences au collège peut être un merveilleux catalyseur éveil à la vocation. Depuis Vitruve et, beaucoup plus tard, Léonard de Vinci, l’ingénieur est un homme de synthèse. Son talent se mesure à une double capacité. La matière à différentes échelles.
Guide 6e - De quoi est fait le monde ? Matière et matériaux. Inventaire ordonné de concepts, constitué de 4 modules logiquement articulés entre eux, ce document propose une structuration intellectuelle relative à la matérialité du monde.
Cet ordonnancement est susceptible d'être décliné en une multitude de démarches concrètes en classe pendant toute l’année de sixième. Les entrées se feront par les phénomènes et/ou par les objets, au choix du professeur. Ce qui importe, c’est de proposer des situations permettant de faire des liens entre les deux, pour aider les élèves à élaborer et approfondir leurs connaissances dans une vision unitaire de la science et de la technologie, en vérifiant les acquis de l'école primaire et en s'appuyant sur eux.
La démarche d'investigation mise en œuvre dans la classe, ne pouvant pas apparaître clairement dans le plan ci-dessous qui ne fait qu’articuler des concepts, est explicitée dans des exemples de séances plus finement détaillées. Yves Quéré 1. 1.1.