

Tpe Le Diamant Luca,Anthony,Correntin,Théo. La cristallisation - Les techniques de cristallogénèse. ← Chapitre précédent :La cristallisationLa croissance en théorie Chapitre suivant : →La cristallisationLes défauts cristallins dans la réalité Les techniques de cristallogénèse Pour cela, on distingue deux types d'approches : On peut prendre un constituant naturel dans un de ses états physiques, la phase (solide, liquide ou gazeuse) est modifiée via des opérations physiques et chimiques successives.

Le cycle de Born-Haber en est un exemple puisque l'on prend du Cl2 gazeux et du Na solide afin de former le cristal NaCl. Diamant et applications. J'ai fait un exposé l'année dernière sur la formation des diamants et leurs utilisations.
Des exemples ont déjà été donnés, à ça je peux ajouter : - pour l'exemple des cellules à enclumes de diamant qui a été donné, on a vu dans notre exposé que les conditions nécessaires à la formation d'un diamant sont très difficiles, et se passent bien loin dans la croûte terrestre.
Le diamant. Reseau, systeme, structure. Formation des cristaux. Lonsdaléite. Un article de Wikipédia, l'encyclopédie libre. structure cristalline de la Lonsdaléite La lonsdaléite est un minéral qui est, avec le diamant et le graphite, l'une des trois formes cristallisées naturelles du carbone.
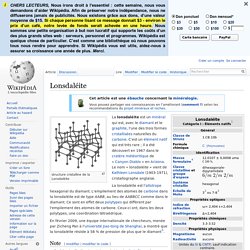
C'est un élément natif qui est très rare ; il a été découvert en 1967 dans le cratère météoritique de « Canyon Diablo » en Arizona. Le nom « lonsdaléite » vient de Kathleen Lonsdale (1903-1971), cristallographe anglaise. En février 2009, une équipe internationale de chercheurs, menée par Zicheng Pan à l'université Jiao-tong de Shanghai, a montré que la lonsdaléite résiste à 58 % de pression de plus que le diamant[5]. Cristaux, Cristallisation et Géométrie cristalline.
Cristaux et Géométrie cristalline Alain Boudet Dr en Sciences Physiques, Thérapeute, Enseignant Résumé: Un cours pour débutants sur la géométrie cristalline.
Le diamant et le quartz sont des cristaux typiques par leur transparence pure et leurs formes géométriques. La géométrie extérieure est la manifestation d'une géométrie intérieure. A qui ce texte s'adresse-t-il? Vous voulez en savoir plus sur les cristaux, mais vous en avez déjà une idée. Ce mot vous fait-il penser à la vaisselle de luxe de grand-mère, aux magnifiques minéraux de la terre, ou encore à une construction atomique géométrique?
Des cristaux et des maths. Des yeux de mouche aux ruches d’abeilles, les structures géométriques des cristaux se retrouvent partout dans la nature.
Comment l’expliquer ? La question taraude de nombreux mathématiciens, dont Mathieu Lewin, qui nous éclaire sur ce sujet intrigant. Quasi-cristal. Un article de Wikipédia, l'encyclopédie libre.
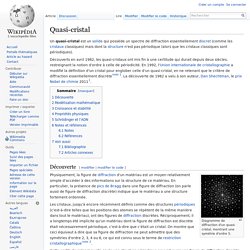
Un quasi-cristal est un solide qui possède un spectre de diffraction essentiellement discret (comme les cristaux classiques) mais dont la structure n'est pas périodique (alors que les cristaux classiques sont périodiques). Découverts en avril 1982, les quasi-cristaux ont mis fin à une certitude qui durait depuis deux siècles, restreignant la notion d'ordre à celle de périodicité. En 1992, l'Union internationale de cristallographie a modifié la définition d'un cristal pour englober celle d'un quasi-cristal, en ne retenant que le critère de diffraction essentiellement discrète[note 1]. La découverte de 1982 a valu à son auteur, Dan Shechtman, le prix Nobel de chimie 2011[1].
Découverte[modifier | modifier le code] Cristal liquide. Un article de Wikipédia, l'encyclopédie libre.
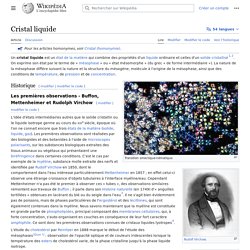
Un cristal liquide est un état de la matière qui combine des propriétés d'un liquide conventionnel et celles d'un solide cristallisé[1],[2]. On exprime son état par le terme de mésophase ou état mésomorphe (du grec « de forme intermédiaire »)[3]. La nature de la mésophase diffère suivant la nature et la structure du mésogène, molécule à l'origine de la mésophase, ainsi que des conditions de température, de pression et de concentration. Transition smectique-nématique Historique[modifier | modifier le code] Les premières observations - Buffon, Mettenheimer et Rudolph Virchow[modifier | modifier le code] Indice de réfraction. Un article de Wikipédia, l'encyclopédie libre.
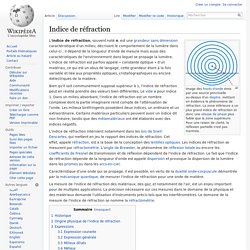
Image des fronts d'onde émis par une source ponctuelle au-dessus d'un dioptre, mettant en évidence le phénomène de réfraction. La zone inférieure a un plus grand indice de réfraction et donc une vitesse de phase plus faible que la zone supérieure. Pour une raison de clarté, la réflexion partielle n'est pas montrée. CRISTALLOGRAPHIE. La cristallisation.

Comme tous les corps simples et combinaisons chimiques, les minéraux peuvent se trouver sous les trois états: gazeux (dans les fumerolles), liquides (dans les magmas et les solutions hydrothermales) et solides. Lorsqu'ils se solidifient, ils le font très souvent sous la forme cristalline. Certains comme l'agathe se présentent sous l'état solide "amorphe", mais ils peuvent aussi se transformer en cristaux au bout d'un temps plus ou moins long. L'état cristallin est donc la forme stable des minéraux solides. Les cristaux se forment soit par refroidissement des minéraux en fusion, ou magmas, minéraux à l'état gazeux ou fumerolles (minéraux formés à hautes températures); soit à partir de solutions hydrothermales (minéraux de basses températures).
Structure cristalline. Structure cristalline Cubique Description: La maille élémentaire (ou solide primitif) du réseau cubique est un cube.
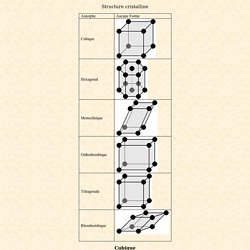
Les trois axes cristallins (a, b, c) sont de longueur égale et les angles qu'ils forment entre eux sont tous égaux à 90°. Les éléments caractéristiques de symétrie sont les axes ternaires, toujours au nombre de 4 (4A3). Le réseau peut être de cubes simples.