

Wikipedia. Un article de Wikipédia, l'encyclopédie libre.
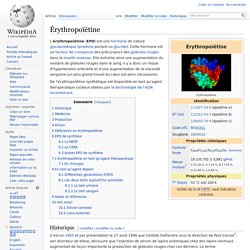
L'érythropoïétine (EPO) est une hormone de nature glycoprotéique (protéine portant un glucide). Cette hormone est un facteur de croissance des précurseurs des globules rouges dans la moelle osseuse. Elle entraîne ainsi une augmentation du nombre de globules rouges dans le sang. Il y a donc un risque d'hypertension artérielle et d'une augmentation de la viscosité sanguine (un plus grand travail du cœur est alors nécessaire). De l'érythropoïétine synthétique est disponible en tant qu'agent thérapeutique coûteux obtenu par la technologie de l'ADN recombinant. Historique[modifier | modifier le code] C'est en 1905 et par présentation le 27 août 1906 que Clotilde Deflandre sous la direction de Paul Carnot[2], son directeur de thèse, découvre que l'injection de sérum de lapins anémiques chez des lapins normaux augmentait de façon importante la production de globules rouges chez ces derniers.
Médecine[modifier | modifier le code] Liste d'hormones. Hautement toxique. EPO, ces effets perdurent jusqu’à 15 à 20 jours après l’arrêt des injections, ce qui rend sa détection difficile.
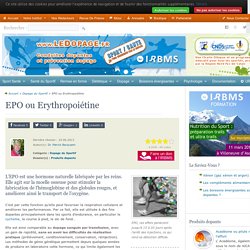
C’est par cette fonction qu’elle peut favoriser la respiration cellulaire et améliorer les performances. Par ce fait, elle est utilisée à des fins dopantes principalement dans les sports d’endurance, en particulier le cyclisme, la course à pied, le ski de fond… Elle est ainsi comparable au dopage sanguin par transfusion, avec un gain de rapidité, sans en avoir les difficultés de réalisation pratique (prélèvement, conditionnement, conservation, réinjection). Les méthodes de génie génétique permettent depuis quelques années de produire en laboratoire cette hormone, ce qui limite également les risques de contamination. Historique Indications thérapeutiques Anémie secondaire à des pathologies graves, telles que l’insuffisance rénale chronique chez les dialysés, les chimiothérapies dans le cadre de cancers sanguins et tumoraux. Conduites dopantes Attention danger ! Combien ça coûte ? Le GW501516, autre produit dopant hautement toxique.
Le GW501516, un produit dopant hautement toxique 4.78/5 - 18 votes Dernière révision : 26.06.2013 Auteur(s): Dr.
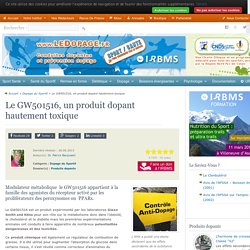
Patrick Bacquaert L’AMA a publié une alerte déclarant que les effets secondaires de la substance interdite GW501516, étaient si graves qu’elle a décidé exceptionnellement d’alerter les tricheurs. Le GW501516 est un produit expérimenté par les laboratoires Glaxo Smith and Kline pour son rôle sur le métabolisme donc dans l’obésité, le cholestérol et le diabète mais les premières expérimentations animales ont conduits à faire apparaître de nombreux potentialités dangereuses et des toxicités.
GW501516 Risques dénoncés par GSK le créateur. La présente est une copie d’une lettre de GlaxoSmithKline Inc.

Veuillez communiquer avec la compagnie pour obtenir copie de toute référence, pièce jointe ou annexe. Renseignements importants au sujet des avis de Santé Canada Le 24 mai 2013. GW501516, usage banalisé. Le Denosumab. Le denosumab (Prolia®) appartient à une nouvelle catégorie de médicaments pour traiter l’ostéoporose appelée inhibiteur du ligand du Rank.
Le denosumab est un traitement anti-ostéoclastique qui empêche le développement et l’activation des ostéoclastes (cellules qui érodent le tissu osseux). Même s’il agit de façon unique par rapport aux autres agents anti-ostéoporotique, le denosumab fait partie de la catégorie de médicaments anti-résorption. Le denosumab réduit le risque de fracture de la colonne, de la hanche et d’autres sites de fractures chez les femmes atteintes d’ostéoporose postménopausique.
Le denosumab peut être utilisé pour réduire le risque de fracture chez les femmes ménopausées atteintes d’ostéoporose. XGEVA 120 mg (denosumab) Monographie 2012 AMGEN Canada. XGEVA 120 mg. Dénosumab 60 mg (Prolia®) & dénosumab 120 mg (Xgeva®) Le dénosumab est un anticorps monoclonal (IgG2) humain qui cible le RANKL, ligand du récepteur RANK.
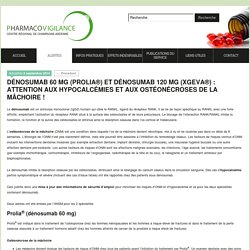
Il se lie de façon spécifique au RANKL avec une forte affinité, empêchant l’activation du récepteur RANK situé à la surface des ostéoclastes et de leurs précurseurs. Le blocage de l’interaction RANK/RANKL inhibe la formation, la fonction et la survie des ostéoclastes et diminue ainsi la résorption osseuse dans l’os cortical et trabéculaire. L’ostéonécrose de la mâchoire (ONM) est une condition dans laquelle l’os de la mâchoire devient nécrotique, mis à nu et ne cicatrise pas dans un délai de 8 semaines. L’étiologie de l’ONM n’est pas clairement définie, mais elle pourrait être associée à l’inhibition du remodelage osseux. Les facteurs de risques connus d’ONM incluent les interventions dentaires invasives (par exemple extraction dentaire, implant dentaire, chirurgie buccale), une mauvaise hygiène buccale ou une autre affection dentaire pré-existante.