

Exergie. Un article de Wikipédia, l'encyclopédie libre.
En thermodynamique, l’exergie est une grandeur permettant de mesurer la qualité d'une énergie. C'est la partie utilisable d'un joule. Le travail maximum récupérable est ainsi égal à l’opposé de la variation d’exergie au cours de la transformation. Un système à l'équilibre thermomécanique ou chimique n'a plus aucune valeur. Plus un système est loin de l'équilibre ambiant, plus il est apte à opérer un changement, aptitude sur laquelle repose l'utilité d'une énergie.
Si selon le premier principe de la thermodynamique la quantité d'énergie se conserve, la qualité de cette énergie, l’exergie, ne peut en revanche que diminuer lors d'une transformation. L'entropie, l'énergie et l'information. Cycle de Carnot. Un article de Wikipédia, l'encyclopédie libre.
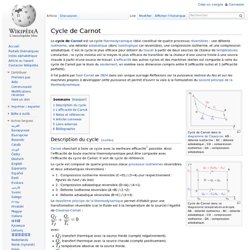
Le est un cycle thermodynamique idéal constitué de quatre processus réversibles : une détente isotherme , une détente adiabatique (donc isentropique car réversible), une compression isotherme, et une compression adiabatique. C'est le cycle le plus efficace pour obtenir du travail à partir de deux sources de chaleur de températures constantes ; le cycle inverse est le moyen le plus efficace de transférer de la chaleur d'une source froide à une source chaude à partir d'une source de travail. L' efficacité des autres cycles et des machines réelles est comparée à celle du cycle de Carnot par le biais du rendement , un nombre sans dimension compris entre 0 (efficacité nulle) et 1 (efficacité parfaite).
Il fut publié par Sadi Carnot en 1824 dans son unique ouvrage et permit d'ouvrir la voie à la formulation du second principe de la thermodynamique . Cycle de Carnot dans le diagramme de Clapeyron . Description du cycle [ modifier ] avec: d'où : P.W. Équipartition de l'énergie. Un article de Wikipédia, l'encyclopédie libre.
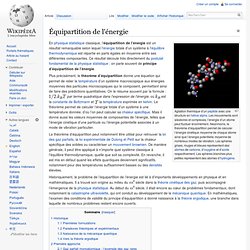
Agitation thermique d’un peptide avec une structure en hélice alpha. Les mouvements sont aléatoires et complexes, l’énergie d’un atome peut fluctuer énormément. Néanmoins, le théorème d’équipartition permet de calculer l’énergie cinétique moyenne de chaque atome ainsi que l’énergie potentielle moyenne de nombreux modes de vibration. Les sphères grises, rouges et bleues représentent des atomes de carbone, d’oxygène et d’azote respectivement. Les sphères blanches plus petites représentent des atomes d’hydrogène. En physique statistique classique, l’équipartition de l’énergie est un résultat remarquable selon lequel l’énergie totale d’un système à l’équilibre thermodynamique est répartie en parts égales en moyenne entre ses différentes composantes.
Par terme quadratique dans l'expression de l'énergie, où est la constante de Boltzmann et la température exprimée en kelvin. Historique[modifier | modifier le code] à la chaleur spécifique où . Et où.