

EXTRAIT - Water, Le Pouvoir Secret de l'Eau (20min) - Officiel. Eau, électromagnétisme et cohérence quantique. On a retrouvé la Mémoire de l'eau, Luc Montagnier, Juillet 2014. Eau. Généralités L'eau est présente sur Terre sous ses trois états : liquide, solide (glace) et gazeux (vapeur d'eau).
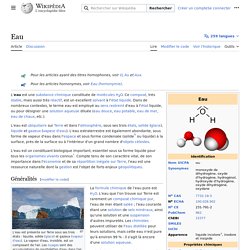
La vapeur d'eau, invisible, est un composant de l'air. Les nuages sont des accumulations de gouttelettes d'eau dans l'air. Majoritairement observable sur Terre à l'état liquide, elle possède les propriétés d'un puissant solvant : elle dissout facilement et solubilise rapidement de nombreux corps sous forme d'ions, ainsi que de nombreuses autres molécules gazeuses[d], et par exemple les composants de l'air, en particulier l'oxygène ou le dioxyde de carbone.
L'expression « solvant universel »[11] est toutefois sujette à maintes précautions, beaucoup de matériaux naturels (roches, métaux, etc.) étant non solubles dans l'eau (dans la plupart des cas ou de manière infime). La surface de la Terre est recouverte à 71 % d’eau[12] (97 % d’eau salée et 3 % d’eau douce dans différents réservoirs) sous différentes formes : Étymologie et usage du mot Cascades de Jonathan’s Run.
Propriétés. Molécule d'eau. Pour un article plus général, voir eau.
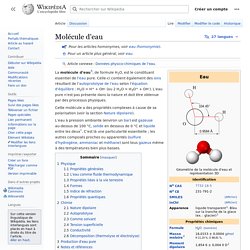
La molécule d’eau[a], de formule H2O, est le constituant essentiel de l’eau pure. Celle-ci contient également des ions résultant de l’autoprotolyse de l’eau selon l’équation d’équilibre : H2O = H+ + OH- (ou 2 H2O = H3O+ + OH-). L’eau pure n’est pas présente dans la nature et doit être obtenue par des processus physiques. Cette molécule a des propriétés complexes à cause de sa polarisation (voir le paragraphe Nature dipolaire). Les chimistes se réfèrent parfois (avec humour) à l’eau avec un nom savant (et justifié) comme du monoxyde de dihydrogène dans des parodies de recherche scientifique sérieuse qui présentent ce produit comme mortellement dangereux et à bannir.
Mémoire de l'eau. Un article de Wikipédia, l'encyclopédie libre.
La mémoire de l’eau est le nom donné, en 1988[1], au cours d'une controverse médiatique, à une hypothèse du chercheur, médecin immunologue, Jacques Benveniste selon laquelle l’eau qui a été en contact avec certaines substances conserve une empreinte de certaines propriétés de celles-ci alors même qu'elles ne s’y trouvent statistiquement plus[Note 1]. Une série d'expériences réalisées pour valider cette hypothèse est alors présentée par les tenants de l'homéopathie (qui pratique une dilution très importante des principes actifs) comme une validation scientifique de celle-ci. Liquide. Un article de Wikipédia, l'encyclopédie libre.
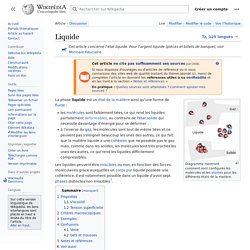
Cet article concerne l'état liquide. Pour l'argent liquide (pièces et billets de banque), voir Monnaie fiduciaire. Propriétés[modifier | modifier le code] Les corps, selon les conditions de température et de pression, peuvent être sous forme de liquide, de gaz ou de solide (voir diagramme de phase). La forme liquide correspond à une forme de moindre énergie que le gaz (l'énergie cinétique des molécules d'un liquide est insuffisante pour rompre les forces qui se matérialisent par la tension superficielle) mais d'énergie supérieure à la forme solide (contrairement au solide, l'énergie cinétique des molécules suffit à les faire se déplacer spontanément les unes par rapport aux autres).
Viscosité[modifier | modifier le code] L'hélium II (« superfluide ») ne possède pas de viscosité du tout. Tension superficielle[modifier | modifier le code] Critères macroscopiques[modifier | modifier le code] Exemples[modifier | modifier le code] Diagramme de phase. Lorsque le système étudié est un mélange de n corps purs, son état physique est défini par les (n-1) proportions indépendantes de ses composants, ainsi que par la température et la pression.
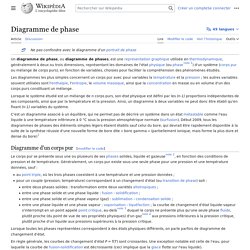
Ainsi, un diagramme à deux variables ne peut donc être établi qu'en fixant (n-1) variables du système. C'est un diagramme associé à un équilibre qui ne permet pas de décrire un système dans un état métastable comme l'eau liquide à une température inférieure à 0 °C sous la pression atmosphérique normale (surfusion). Début 2009, tous les diagrammes de phases des éléments simples légers étaient établis sauf celui du bore, qui devrait être rapidement disponible à la suite de la synthèse réussie d'une nouvelle forme de bore dite « bore gamma » (partiellement ionique, mais forme la plus dure et dense du bore)[1] Diagramme d'un corps pur[modifier | modifier le code] Lorsque toutes les phases représentées correspondent à des états physiques différents, on parle parfois de diagramme de changement d'état. avec :